小奕说药 | 开发用于皮下注射的超高浓度人免疫球蛋白制剂
研究背景
• 需求:蛋白类生物制剂(如多克隆抗体hIgG)在皮下注射时需高浓度(如武田现有产品Cuvitu®为200 mg/mL),但高浓度会导致溶液黏度急剧上升和聚集显著增加,超出FDA对皮下注射黏度(≤50 cP)和体积(≤1.5 mL)的限制。
• 挑战:传统方法(如结晶悬浮液或有机溶剂)存在制备周期长、稳定性差或不符合法规的问题。
• 目标:开发一种新型非晶态悬浮液制剂,通过喷雾干燥技术制备高浓度(最高400 mg/mL)的hIgG微粒,并解决黏度与可注射性的难题。
研究方法
喷雾干燥技术
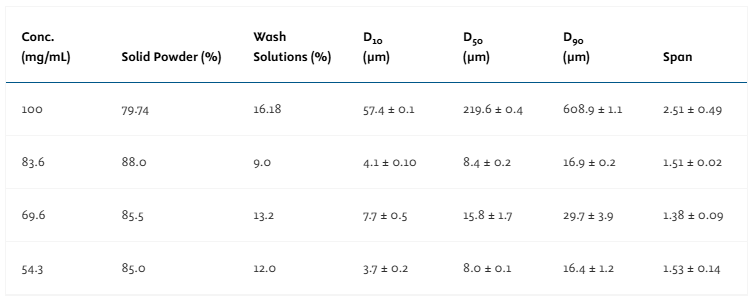
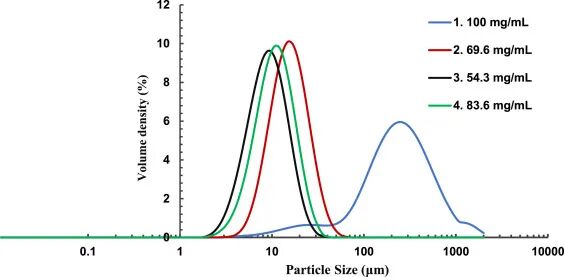
• 将hIgG溶液(50 mg/mL)喷雾干燥为固体粉末(SDS),优化参数(入口温度120°C,出口温度54°C),获得粒径90% <20 μm的微粒,单体含量93%,聚集体仅0.3%。
• 喷雾干燥产物收率达85.5%,且热稳定性良好(DSC显示无降解)。
悬浮液配方设计
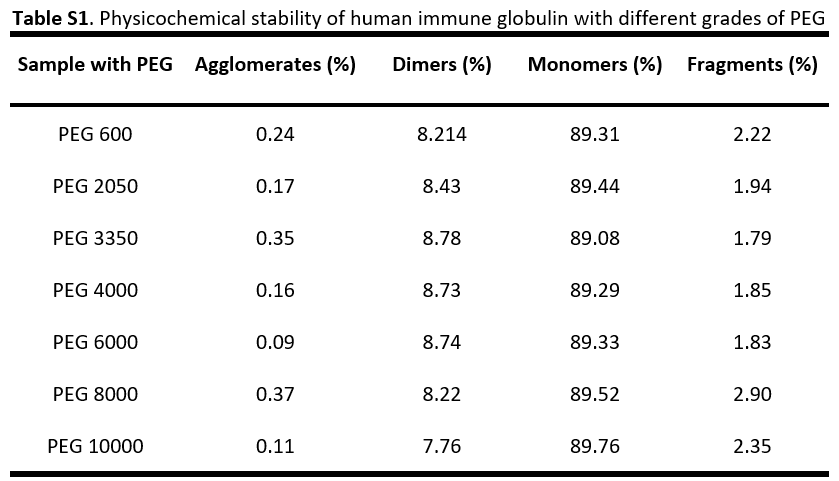
• 分散介质:以10% hIgG溶液(含250 mM甘氨酸缓冲液)为基础,添加PEG 6000(优化分子量)和NaCl形成饱和介质,抑制微粒溶解。
• 添加剂:天冬氨酸(Asp)和尿素(URE)作为“分子润滑剂”,与PEG协同降低黏度。
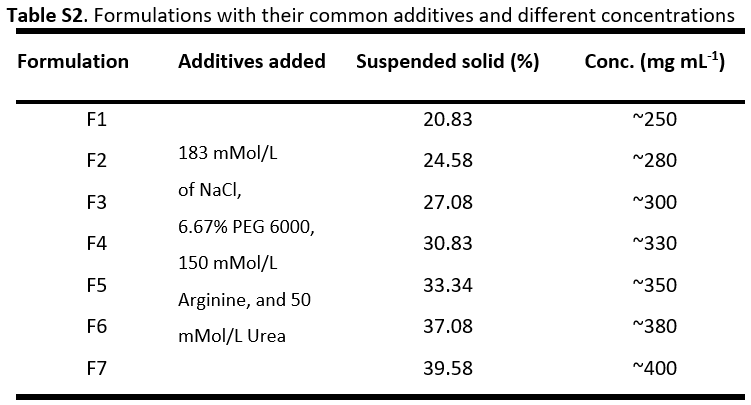
• 配方浓度:从250 mg/mL至400 mg/mL,逐步优化组分比例(详见表S2)。

关键结果
黏度与流变特性:
• 300 mg/mL悬浮液黏度为128 cP,380 mg/mL为284 cP,400 mg/mL黏度显著升高(>1000 cP),但剪切增稠特性使其仍可注射。
• 非牛顿流体行为:低剪切速率下黏度极高,但高剪切(注射过程)下流动性改善。
可注射性测试
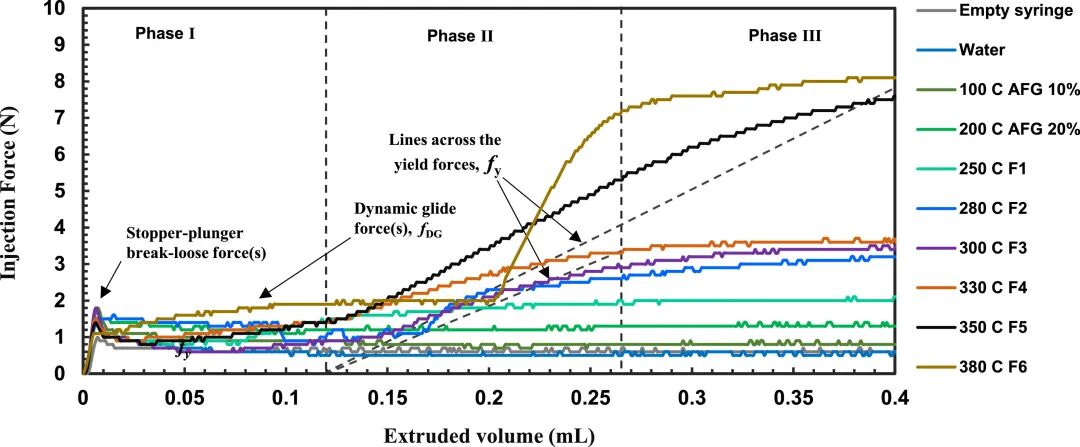
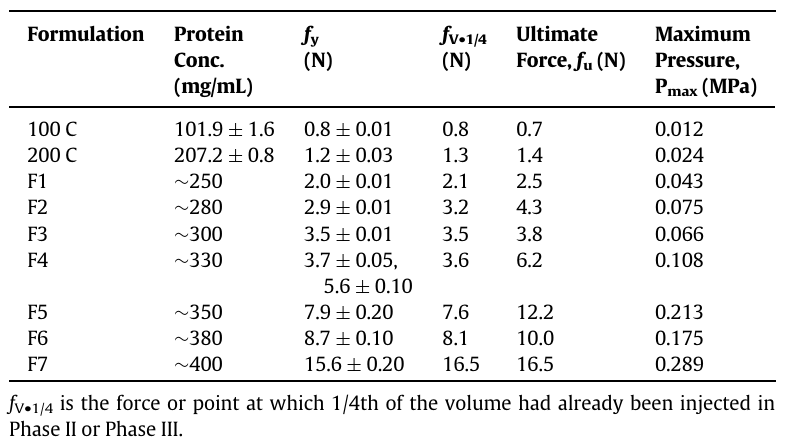
• 使用24G针头,注射力随浓度增加:300 mg/mL需3.8 N,400 mg/mL需16.5 N(远低于女性医师推荐上限40 N)。
• 注射过程分为四个阶段(图8-9),其中“平台期”(Phase III)显示稳定流动,表明配方机械均质性良好。
物理化学稳定性
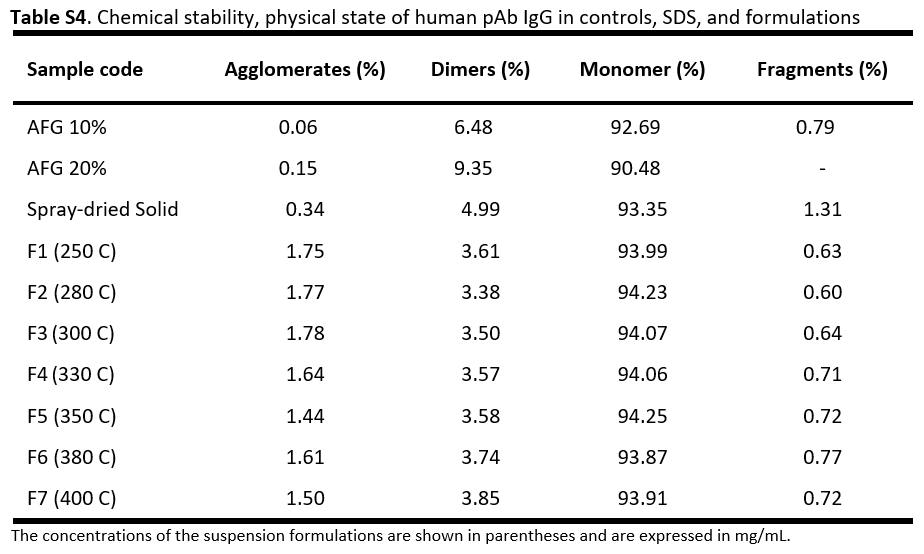
• 尺寸排阻色谱(SEC)显示单体含量>90%,聚集体<0.3%,符合药典标准。
• 喷雾干燥粉末在120°C下稳定,悬浮液在长期储存中无明显聚集。
总结
该研究通过喷雾干燥和配方优化,成功开发出超高浓度hIgG悬浮液,突破了传统黏度限制,证明了“可注射性”而非单纯黏度是临床可行的关键参数。这一技术为生物制剂的高浓度皮下给药提供了新思路。
突破与意义
技术突破
• 首次实现400 mg/mL hIgG悬浮液的皮下注射,突破传统黏度限制。
• 提出“黏度-可注射性悖论(VIP)”:高黏度配方通过优化流变特性仍可注射。
应用价值
• 为高剂量抗体药物(如免疫疗法)提供皮下给药方案,提高患者依从性。
• 喷雾干燥与悬浮液技术可扩展至其他生物制剂。
局限与未来方向
局限性
• 400 mg/mL配方注射力较高(16.5 N),需临床评估患者疼痛感受。
• 长期化学稳定性(如质谱分析)和降解研究尚未完成。
未来工作
• 开展临床前稳定性测试(如强制降解实验)。
• 优化添加剂组合以进一步降低黏度。
参
考
文
献
Yadav J, Uddin S, Civati F, Ma W, Liebminger A, Teschner W, André G, Trout BL, Braatz RD, Myerson AS. Developing ultra-high concentration formulations of human immune globulins for subcutaneous injectables. J Pharm Sci. 2025 Mar;114(3):1605-1614.
推荐阅读
关于奕安济世
About HJB
奕安济世具有丰富的细胞系开发、工艺开发、临床样品生产及放行、IND/BLA申报的全流程经验。奕安济世在杭州拥有工艺开发中心及符合cGMP标准的原液及成品生产车间,通过技术的不断创新及稳定的连续化生产工艺,可极大缩短工艺开发进程和降低生产成本,为生物药创新合作伙伴提供优质、可靠、快速的CDMO服务。
我们与客户共赢,我们与时代共进。
业务咨询:
BD@hjbbio.com | 13601691087 | 0571-2827 9502*8555
















发表评论